
Алгоритм диагностики и лечения головной боли
Согласно данным Всемирной организации здравоохранения, каждый второй взрослый хотя бы один раз на протяжении года страдает от головной боли (ГБ), а 1,7‒4% взрослого населения мира страдают от ГБ, продолжающейся 15 или более дней ежемесячно [1]. Это обусловливает актуальность проблемы и частоту встречаемости таких пациентов на приеме у невролога.
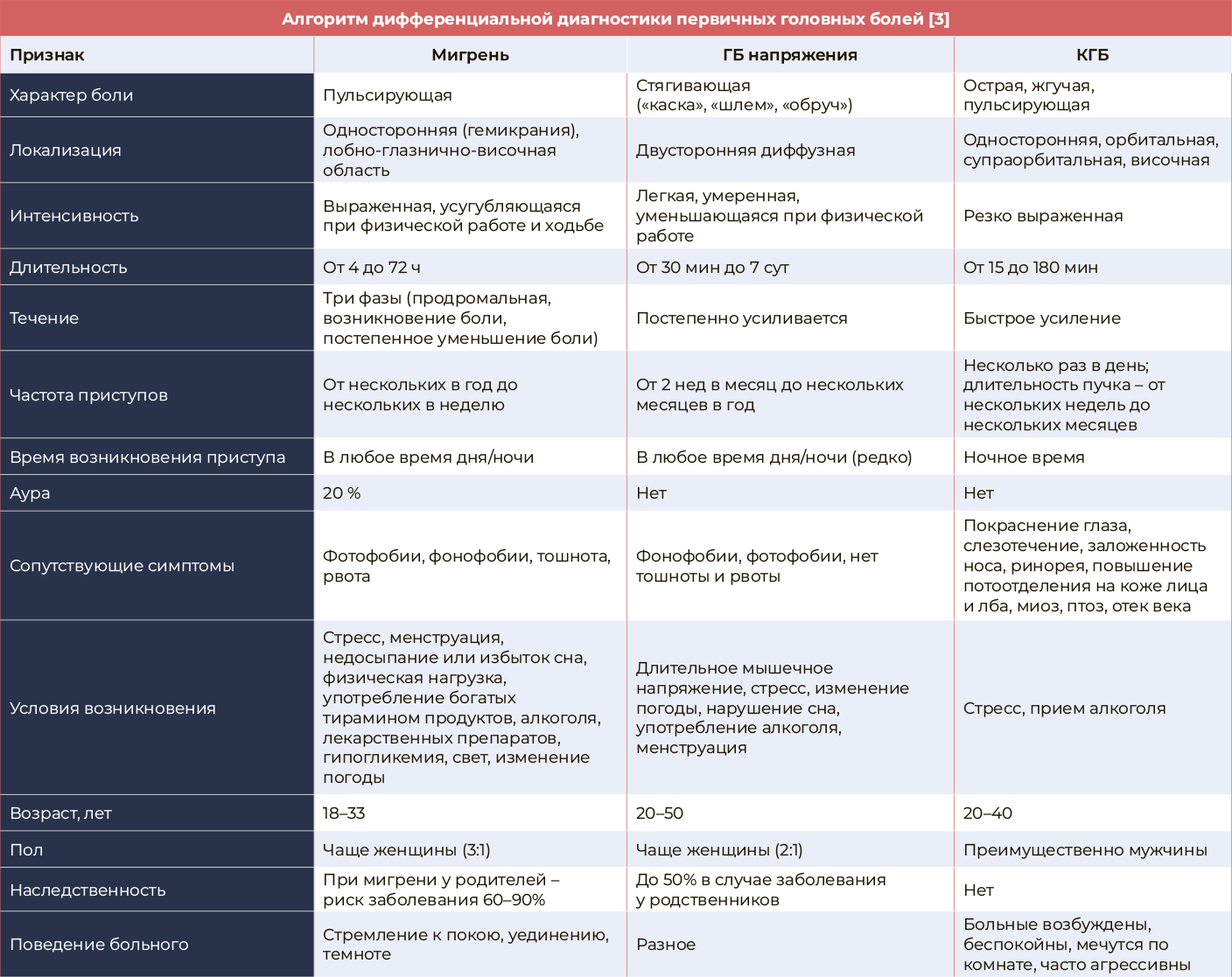
Клиницисту важно ориентироваться в многообразии видов ГБ для составления индивидуальной схемы лечения пациента. В частности, нужно уточнить характер первичной ГБ, к которой относят мигрень, ГБ напряжения, кластерную ГБ (КГБ) и другие тригеминальные вегетативные (автономные) цефалгии [2].
Патогенетические аспекты развития мигрени
Именно мигрень занимает 6-е место среди ведущих причин снижения качества жизни людей в мире, а распространенность мигрени в мире достигает 14% [4, 5]. Согласно современным представлениям, мигрень – это хроническое нейроваскулярное заболевание с наследственной предрасположенностью. Доминирующим звеном патогенеза становится развитие периваскулярного нейрогенного воспаления мозговых сосудов, в основном сосудов твердой мозговой оболочки. Повышенная возбудимость нейронов коры головного мозга и тригемино-васкулярной системы гипоталамуса, корковых и некоторых других структур головного мозга, характерная для таких пациентов, усиливается на фоне воздействия эндогенных и экзогенных мигренозных триггеров. Активируются тригеминальный ганглий, сенсорные спинномозговые ядра тройничного нерва и волокна тройничного нерва, иннервирующие сосуды тригемино-васкулярных волокон. Это сопровождается выбросом болевых провоспалительных пептидов-вазодилататоров (например, кальцитонин-ген-родственного пептида ‒ CGRP), нейрокинина А и субстанции Р. В результате вазодилатации и нейрогенного воспаления в стенке сосудов твердой мозговой оболочки активируются болевые рецепторы, импульсация от которых поступает в сенсорную кору головного мозга ‒ формируется ощущение ГБ. Гипервозбудимость ноцицептивных структур и постепенное истощение противоболевой системы постепенно приводят к учащению приступов мигрени и к хронизации процесса [4].
Кластерная головная боль
Распространенность КГБ на протяжении всей жизни среди взрослых всех возрастов, согласно результатам исследований, составляет 124 на 100 тыс., или примерно 0,1%. Несмотря на то, что это может показаться редкостью, пациента мучает самая страшная ГБ, и до недавнего времени очень сложно было назначить адекватную терапию [6].
Особая проблема здравоохранения ‒ отсроченность постановки диагноза КГБ, ведь около половины случаев КГБ не диагностированы. В британском исследовании показано, что врачами общей практики диагноз КГБ ставится лишь в 20% случаев. Время от дебюта заболевания до постановки правильного диагноза составляет в разных странах от 2,6 до 9 лет. Эти неутешительные данные подтверждают важность включения КГБ в образовательные программы для специалистов здравоохранения [6].
Диагностические критерии КГБ в соответствии с 3-й редакцией Международной классификации головных болей (МКГБ-3) [6]:
A. Минимум пять атак, отвечающих критериям B‒D.
B. Приступы, характеризующиеся сильной или очень сильной односторонней болью орбитальной, супраорбитальной и/или височной локализации длительностью от 15 до 180 мин при отсутствии лечения.
C. Одно или оба из следующих условий:
1. Одно или оба из следующих условий:
2. Беспокойство или ажитация.
D. Частота приступов ‒ от 1 до 8 в день.
E. Лучше не объясняется другим диагнозом по МКГБ-3.
Эпизодическая форма ‒ наиболее распространенная (от 80 до 90% пациентов с КГБ). Для нее характерно чередование периодов приступов (кластерных периодов) и периодов ремиссии. Во время кластерного периода происходит от 1 до 8 приступов в день, а сам период может длиться от 7 дней до 12 мес. В период ремиссии обычно нет никаких симптомов. Хроническая форма КГБ диагностируется, если кластерный период существует более 12 мес без ремиссии или если ремиссия длится менее 3 мес. [6].
Возможности терапии мигрени и КГБ
Терапия мигрени
При купировании приступов мигрени продемонстрировали свою эффективность широко известные в профессиональном сообществе триптаны [2]. Антимигренозные препараты влияют на обмен серотонина, ингибируют выброс вазоактивного пептида, блокируют импульсацию ноцицептивных путей. Среди триптанов достойное место занимает золмитриптан, действующее вещество препарата Эксенза®. Его особенностью является интраназальная форма выпуска, позволяющая сократить время наступления эффекта до 15 мин от начала использования [7, 8]. К другим классам медикаментозных средств для купирования мигренозного приступа относят анальгетики и препараты дигидроэрготамина [3].
Существуют и профилактические схемы терапии мигрени. Их назначают при частых (2 и более в месяц) приступах, тяжелых эпизодах, вызывающих потерю трудоспособности на срок более 3 дней, а также при редких приступах ГБ, вызывающих преходящие неврологические расстройства. Профилактическая терапия может сочетаться с немедикаментозными методами [3].
Терапия КГБ
Два направления терапии КГБ:
Терапия острых приступов КГБ
Для купирования боли используются ингаляции 100% кислорода (необходимая скорость ‒ 6‒12 л/мин, уровень доказательности ‒ УД А).
В качестве альтернативы рекомендованы триптаны: золмитриптан 5‒10 мг в таблетках (УД В), суматриптан 6 мг в форме подкожных инъекций (УД A, не зарегистрирован в Российской Федерации), золмитриптан назальный спрей 5 мг (УД A, до недавнего времени был не зарегистрирован в Российской Федерации) [6].
Сегодня в арсенале врачей существует золмитриптан в форме назального спрея – препарат Эксенза® [9]. Согласно результатам исследования, через 30 мин после применения препарата происходит уменьшение интенсивности КГБ с сильного/умеренного уровня до легкого уровня/полного купирования [9].
Профилактическая терапия КГБ
Верапамил ‒ препарат выбора для профилактики эпизодической и хронической КГБ (УД A). Лечение необходимо начинать с суточной дозы 240 мг. Большинство пациентов отвечают на 240‒480 мг/сут, но некоторым пациентам требуется суточная доза до 960 мг. Эффект от препарата проявляется в течение 2‒3 нед. После окончания кластерного периода резко прекращать прием верапамила нельзя, доза снижается постепенно (2‒4 нед, все зависит от дозы) до полной отмены препарата [6].
Литература:
1. Всемирная организация здравоохранения. Головные боли. https:// www.who.int/ru/news-room/fact-sheets/detail/headache-disorders/Дата обращения: 20.01.2023.
2. Международная классификация головной боли (3-е издание, 2018). Адаптированная русскоязычная версия.
3. Кадыков А.С., Шахпаронова Н.В. Алгоритмы диагностики и лечения мигрени. Нервные болезни. 2008; 3: 23‒6.
4. Мигрень. Клинические рекомендации. 2021. Россия.
5. Осипова В.В., Филатова Е.Г., Артеменко А.Р. Диагностика и лечение мигрени: рекомендации российских экспертов. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2017; 117 (1‒2): 28‒42.
6. Азимова Ю.Э., Ужахов А.М., Ващенко Н.В., Скоробогатых К.В., Коробкова Д.З., Климов Е.А., Кукушкин М.Л. Кластерная головная боль: современное состояние проблемы. Российский журнал боли. 2021;19(3):39 44.
7. Dodick D, Brandes J, Elkind A et al. Speed of onset, efficacy and tolerability of zolmitriptan nasal spray in the acute treatment of migraine: a randomised, double-blind, placebo-controlled study. CNS Drugs 2005; 19 (2): 125‒36. DOI: 10.2165/00023210-200519020-00003 ]Додик Д., Брандес Я., Элкинд А. и др. Скорость начала действия, эффективность и переносимость назального спрея золмитриптана при остром лечении мигрени: рандомизированное двойное слепое плацебо-контролируемое исследование. Препараты ЦНС. 2005; 19 (2): 125‒36. DOI: 10.2165/00023210-200519020-00003]
8. Nahas SJ. Zolmitriptan for Early Onset of Action in Acute Migraine Attacks. touchREVIEWS in Neurology. 2021; 17 (2): 74–6. DOI: 10.17925/USN.2021.17.2.74 [Нахас С.Дж. Золмитриптан как препарат раннего начала действия при острых приступах мигрени. Обзоры в неврологии. 2021; 17 (2): 74–6. DOI: 10.17925/USN.2021.17.2.74]
9. Инструкция по медицинскому применению препарата Эксенза®.
10.Бойко А.Н. Головная боль: введение в проблему. https://medi.ru/info/12361/




